Los semiconductores son componentes esenciales en la electrónica moderna, utilizados en una amplia variedad de dispositivos como computadoras, teléfonos celulares y televisores. En este artículo, exploraremos los conceptos básicos de los semiconductores, explicando cómo funcionan y por qué son tan importantes en la tecnología actual. ¡Acompáñanos en este fascinante viaje al mundo de los semiconductores!
Para entender cómo funcionan los diodos, transistores u otros circuitos integrados, primero hay que examinar el semiconductor, un material que no es ni conductor ni aislante.
Antes de conocer los semiconductores, comprendamos qué hace que un material sea conductor o aislante.
conductor
Todos sabemos que el cobre es un buen conductor. La razón es obvia cuando observamos su estructura atómica.

El núcleo de un átomo de cobre tiene 29 protones (carga positiva). 29 electrones (carga negativa) giran alrededor del núcleo. Hay 2 electrones en la primera órbita, 8 electrones en la segunda, 18 en la tercera y 1 electrón en la órbita exterior.
En electrónica lo único que importa es la órbita exterior porque determina la conductividad del átomo. También dice trayectoria valencia.
Tarifa neta
Para encontrar la carga neta de un átomo, definimos el núcleo de un átomo como el núcleo y sus orbitales internos.
El núcleo de un átomo de cobre tiene un núcleo (+29 protones) y las tres primeras órbitas (-28 electrones). Por tanto, el núcleo de un átomo de cobre tiene una carga neta de +1 (+29 protones -28 electrones).
La siguiente figura muestra el núcleo y la órbita de valencia de un átomo de cobre.
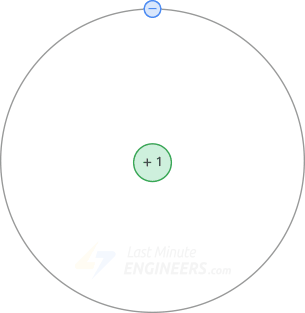
electrones libres
Dado que el núcleo sólo tiene una carga neta de +1, la atracción entre el núcleo y el electrón de valencia es muy débil. Incluso un voltaje nominal puede desalojar fácilmente este electrón de un átomo de cobre y hacer que fluya a través del material. Por esta razón, al electrón de valencia se le suele denominar electrón libre. Y el flujo de estos electrones libres se llama Actual.
El número de electrones libres en el cobre, como en otros metales, lo convierte en un buen conductor de la electricidad.
Aisladores
El neón es un ejemplo del mejor aislante. Veamos su estructura atómica.
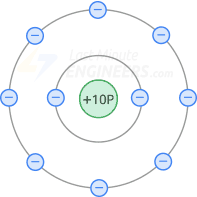
Un átomo de neón tiene 10 protones y 10 electrones. La primera órbita contiene dos electrones y los ocho electrones restantes están en la órbita de valencia.
El núcleo de un átomo de neón tiene una carga neta de +8 porque contiene 10 protones en el núcleo y 2 electrones en la primera órbita. La siguiente figura muestra el diagrama nuclear de un átomo de neón.
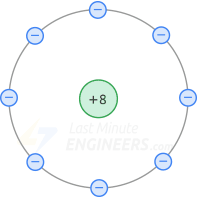
Dado que el núcleo tiene una carga neta de +8, la atracción interna de los electrones de valencia es muy grande. Por tanto, debido a la falta de electrones libres, los aislantes no son conductores.
Si se aplica un voltaje suficientemente alto a un aislante, la fuerza es tan grande que los electrones de valencia son literalmente arrancados de sus átomos. Esto lleva a una línea. En el aire lo verás como un arco o un rayo. En el caso de materiales sólidos, el calor generado provoca la carbonización del material.
semiconductor
Un semiconductor es un elemento que no es ni buen conductor ni buen aislante. Como era de esperar, los mejores semiconductores tienen cuatro electrones de valencia.
El silicio es un ejemplo de semiconductor. Veamos su estructura atómica.
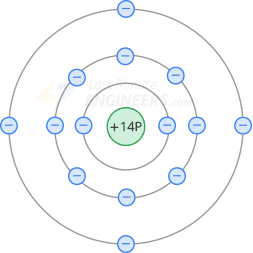
Un átomo de silicio tiene 14 protones y 14 electrones. La primera órbita contiene dos electrones y la segunda órbita contiene ocho electrones. Los cuatro electrones restantes están en la órbita de valencia.
El núcleo de un átomo de silicio tiene una carga neta de +4 porque contiene 14 protones en el núcleo y 10 electrones en las dos primeras órbitas. La siguiente figura muestra el diagrama nuclear de un átomo de silicio.
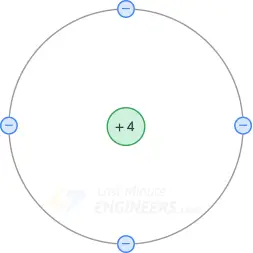
La conductividad del átomo depende del número de electrones de valencia. Si un átomo tiene un solo electrón de valencia, es el mejor conductor. Si un átomo tiene ocho electrones de valencia, ese átomo es el mejor aislante.
Como puedes ver, un átomo de silicio tiene cuatro electrones de valencia, lo que sitúa su conductividad eléctrica entre la de un conductor y la de un aislante. Esto convierte al silicio en un semiconductor.
cristales de silicio
Cuando los átomos de silicio se combinan para formar un cristal, se organizan siguiendo un patrón sistemático. Cada átomo de silicio comparte sus electrones de valencia con cuatro átomos vecinos, por lo que cada átomo tiene ocho electrones en su órbita de valencia.
La siguiente figura muestra cómo un átomo de silicio comparte electrones con cuatro vecinos.
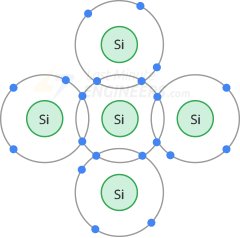
Enlaces covalentes
Al ser compartidos, los electrones de valencia ya no pertenecen a ningún átomo. Estos electrones de valencia compartidos son atraídos por los átomos vecinos con fuerzas iguales y opuestas, lo que hace que formen un enlace. A este tipo de enlace químico lo llamamos Enlace covalente.
La siguiente figura muestra el concepto de enlaces covalentes, donde cada línea recta representa un electrón compartido.

Esta atracción en direcciones opuestas mantiene unidos los átomos de silicio y les da fuerza.
Los agujeros
A temperatura ambiente, la energía térmica del aire hace que los átomos de un cristal de silicio vibren. Estas oscilaciones sacan al electrón de la órbita de valencia. Este electrón libre comienza a moverse aleatoriamente a través del cristal.
La pérdida del electrón crea una brecha en el camino de valencia llamada Agujero. Este hueco se comporta como una carga positiva porque la pérdida de un electrón crea un ion positivo.
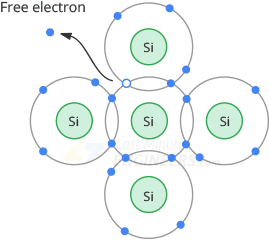
Cuando un electrón libre llega a las inmediaciones del agujero, es atraído hacia el agujero y cae en él. El proceso de fusión de un electrón libre y un hueco se llama Recombinación.
Flujo de electrones y huecos libres.
Conectemos una batería a través de un cristal de silicio puro. Supongamos que la energía térmica creó un electrón libre y un agujero.
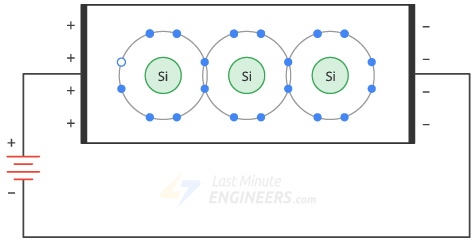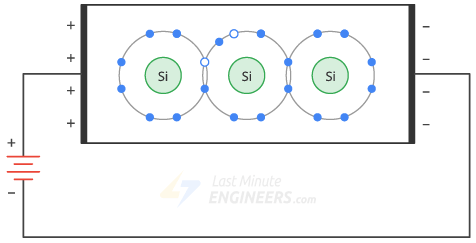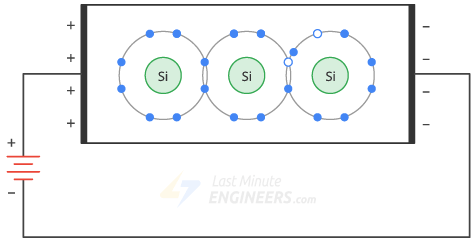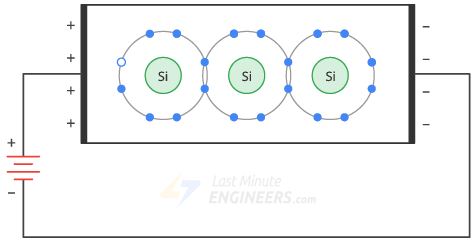
El voltaje aplicado obliga a los electrones libres a fluir hacia la izquierda y a los huecos a fluir hacia la derecha. Cuando los electrones libres llegan al extremo izquierdo del cristal, penetran el cable exterior y fluyen hacia el terminal positivo de la batería.
Por otro lado, los electrones libres en el terminal negativo de la batería fluyen hacia el extremo derecho del cristal. Penetran en el cristal y se vuelven a conectar con agujeros que han llegado al extremo derecho del cristal.
De esta forma se crea un flujo constante de electrones libres y huecos en el interior del semiconductor.
A menudo se mencionan los electrones libres y los huecos. transportador porque transportan una carga de un lugar a otro.
Dopando un semiconductor
En un cristal de silicio puro, cada átomo de silicio utiliza cuatro electrones de valencia para unirse con sus átomos vecinos. Esto reduce la cantidad de electrones disponibles para la conducción. Esto hace que tenga un efecto aislante.
Para aumentar el número de huecos y electrones libres en un cristal de silicio y así aumentar su conductividad, es necesario dopar el cristal.
dopaje Es el proceso de agregar impurezas a un cristal de silicio puro para cambiar su conductividad eléctrica. Y la impureza añadida se llama dopante.
Cuantas más impurezas se añaden, más electrones libres y huecos quedan, lo que provoca un aumento de la conductividad. Es decir, un semiconductor ligeramente cerrado tiene una resistencia alta, mientras que un semiconductor muy dopado tiene una resistencia baja.
¿Cómo se dopa un cristal de silicio?
En primer lugar, se funde un cristal de silicio puro. Esto rompe los enlaces covalentes y convierte el silicio de sólido a líquido. Para aumentar el número de electrones libres, se añaden átomos pentavalentes al silicio fundido. Y para aumentar el número de huecos se añaden átomos de tritán. Una vez que se enfría, se convierte en una estructura cristalina sólida.
semiconductor tipo n
Silicio es el nombre que se le da al silicio que se dopa para aumentar el número de electrones libres. semiconductor tipo ndonde n significa negativo.
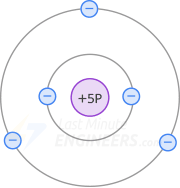
Para aumentar el número de electrones libres, se añaden al silicio impurezas pentavalentes como fósforo, antimonio o arsénico. Los átomos pentavalentes, como su nombre indica, tienen cinco electrones de valencia. La siguiente figura muestra un átomo de fósforo.
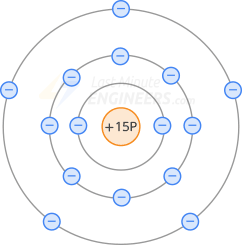
En los semiconductores de tipo n, hay un átomo pentavalente en el centro rodeado por cuatro átomos de silicio. Como sabemos, un átomo pentavalente tiene cinco electrones de valencia. Como antes, los átomos de silicio vecinos comparten cuatro electrones con un átomo pentavalente. Pero esta vez queda un electrón extra (ya que la órbita de valencia no puede contener más de ocho electrones).
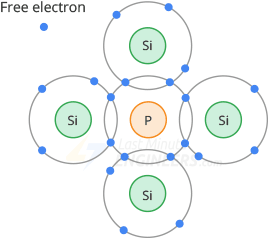
Debido a que cada átomo pentavalente en un cristal de silicio produce un electrón libre, el material dopado resultante tiene una gran cantidad de electrones libres.
En un semiconductor tipo n, los electrones libres se llaman porque el número de electrones libres es mayor que el de huecos. Empresa de transporte mayoritaria y los agujeros se llaman Empresa de transporte minoritaria..
Debido a que las impurezas pentavalentes donan un electrón adicional al cristal de silicio, a menudo se las denomina «». Contaminación del donante.
semiconductor tipo p
Silicio es el nombre que se le da al silicio que se dopa para aumentar el número de agujeros semiconductor tipo pdonde p significa positivo.
Para aumentar el número de agujeros, se añaden al silicio impurezas triactivas como aluminio, boro o galio. Los átomos trivalentes, como su nombre indica, tienen tres electrones de valencia. La siguiente figura muestra un átomo de boro.
En el semiconductor tipo p hay un átomo trivalente en el centro rodeado por cuatro átomos de silicio. Dado que el átomo trivalente originalmente solo tenía tres electrones de valencia y cada vecino comparte un electrón, solo hay siete electrones en la órbita de valencia. Esto significa que hay un agujero en la órbita de valencia de cada átomo trivalente.
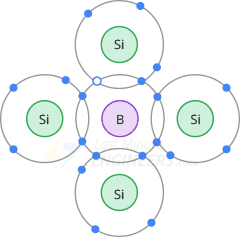
Debido a que cada átomo trivalente en un cristal de silicio crea un agujero, el material dopado resultante tiene una gran cantidad de agujeros.
En un semiconductor tipo p, los huecos se llaman porque el número de huecos es mayor que el de electrones libres. Empresa de transporte mayoritaria y llamados electrones libres Empresa de transporte minoritaria..
Un átomo trivalente también se llama An. átomo aceptorporque cada hueco que aporta puede aceptar un electrón libre durante la recombinación.
Siga adelante
En el siguiente tutorial, veremos cómo dopar un único cristal de silicio con material tipo p en un lado y material tipo n en el otro lado para formar una unión PN que puede usarse para fabricar un diodo.
[automatic_youtube_gallery type=»search» search=»Conceptos básicos de semiconductores
» limit=»1″]
Conceptos básicos de semiconductores
Para comprender cómo funcionan diodos, transistores o cualquier circuito integrado, primero debes estudiar el semiconductor, un material que no es ni un conductor ni un aislante.
Conductor
Todos sabemos que el cobre es un buen conductor. La razón es obvia cuando observamos su estructura atómica.
El núcleo de un átomo de cobre tiene 29 protones (carga positiva). 29 electrones (carga negativa) giran alrededor del núcleo. Hay 2 electrones en la primera órbita, 8 electrones en la segunda, 18 en la tercera y 1 electrón en la órbita exterior.
Aislantes
El neón es un ejemplo de un mejor aislante. Veamos su estructura atómica.
Un átomo de neón tiene 10 protones y 10 electrones. La primera órbita contiene dos electrones y los ocho electrones restantes están en la órbita de valencia.
Semiconductores
Un semiconductor es un elemento que no es ni un buen conductor ni un buen aislante. Los mejores semiconductores tienen cuatro electrones de valencia.
El silicio es un ejemplo de un semiconductor. Veamos su estructura atómica.
Un átomo de silicio tiene 14 protones y 14 electrones. La primera órbita contiene dos electrones y la segunda órbita contiene ocho electrones. Los cuatro electrones restantes están en la órbita de valencia.
Enlaces covalentes
Debido al intercambio, los electrones de valencia ya no pertenecen a un solo átomo. Estos electrones de valencia compartidos son atraídos por átomos vecinos con fuerzas iguales y opuestas, lo que hace que formen un enlace. Llamamos a este tipo de enlace químico un enlace covalente.
Dopaje de un semiconductor
Para aumentar el número de agujeros y electrones libres en un cristal de silicio, y así aumentar su conductividad, es necesario dopar el cristal. El dopaje es el proceso de añadir impurezas a un cristal de silicio puro para alterar su conductividad eléctrica. Y la impureza que se añade se llama dopante.
Para obtener más información detallada sobre este tema, te invito a leer el articuló inspirador original en Electronics Tutorials
¡Qué buen resumen sobre los semiconductores! Me aclaró bastante el tema y ahora siento que estoy un poco menos perdido en el mundo de la tecnología. ¡Gracias por compartir esta información!
¡Gracias por simplificar los conceptos básicos de semiconductores! Realmente me ayudó a comprender mejor cómo funcionan en la electrónica moderna. ¡Excelente artículo!
¡Me encantó el artículo! Los conceptos básicos de semiconductores son más fáciles de entender ahora. ¡Gracias por la explicación sencilla y clara!
¡Interesante explicación sobre los semiconductores! Nunca entendí bien cómo funcionaban, ahora todo tiene más sentido. ¡Gracias por la info!